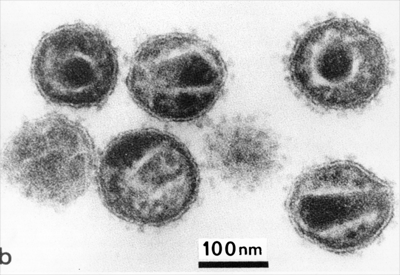
HIV يك رتروويروس و عضوي از زير خانواده لنتي ويريده است و داراي بسياري از خصوصيات فيزيكي – شيميايي مشخص اين خانواده مي باشد . خصوصيت مورفولوژيك منحصر به فرد HIV، وجود يك نوكليوتيد استوانه اي در ويريون بالغ است . نوكلويتيد ميله اي شكل مشخص ، در تصاوير ميكروسكوپ الكتروني از ويروس هاي خارج سلولي كه با زاويه مناسب برش داده شده اند ، قابل مشاهده مي باشد .
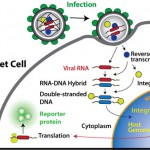
ژنوم RNA لنتي ويروس ها ، نسبت به رتروويروس هاي ترانس فرم كننده ، پيچيده تر است . اين ويروس ، هر 3 ژن مورد نياز براي تكثير رتوويروس هاgag ، pro ، pol ، و –env را دارا مي باشد . تا 6 ژن اضافي ديگر نيز وجود دارند كه بيان ژن هاي ويروسي را تنظيم مي كنند و در بيماري زايي ويروس در بدن اهميت دارند .اگرچه توالي اين ژن هاي اضافي در بين لنتي ويروس ها ، شباهت اندكي دارند ، اما عملكرد آن ها يكسان مي باشد ( ويروس هاي گربه سانان و پستانداران سم دار ، تنها داراي 3 ژن اضافي هستند ( . يك پروتيين تكثيري مرحله ي زودرس ، به نام پروتيين Tat ، در transactivation ( فعال سازي متقاطع ) نقش دارد ، در حالي كه يك فرآورده ژني ديگر در فعال سازي نسخه برداري از ساير ژن هاي ويروسي دخالت دارد . transactivation ( فعال سازي متقاطع ) درHIV بسيار كارآمد است وممكن است ، تا حدودي ، مسول ماهيت تهاجمي عفونت HIV باشد . پروتيين Rev براي بيان پروتيين هاي ساختماني ويروس ، ضروري است .Rev، خروج نسخه هاي ويروسي برش نخورده را از هسته سلول ، تسهيل مي كند . ازmRNA برش نخورده در طي مرحله انتهايي تكثير ويروس ، پروتيين هاي ساختماني توليد مي شوند . پروتيين Nef توليد كموكين هايي را از ماكروفاژ ها تحريك مي كند كه قادرند سلول هاي Tدر حال استراحت را فعال سازند و توليد وتكثير HIV را امكان پذير كنند . وجود ژن nef براي بيماري زا بودن SIV 0ويروس نارسايي ايمني ميمون ) ضروري است . پروتيين Vpr انتقال كمپلكس ويروسي پيش از الحاق به هسته را به داخل هسته افزايش مي دهد و سلول ها را نيز در مرحله G2 چرخه سلولي متوقف مي كند . پروتيين Vif ، عفونت زايي را تسهيل مي كند ، اين كار را با سركوب اثرات پروتيين سلولي مهاري ( كه در برخي سلول هاي انسان وجود دارند ) انجام مي دهد .
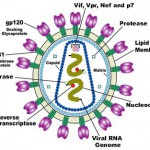
ويروس هاي متعدد جداسازي شده HIV ، كاملاَََ يكسان نيستند ، و به نظر مي آيد كه طيفي از ويروس هاي مشابه را تشكيل مي دهند . جمعيت هاي نا همگوني از ژنوم ويروس در يك فرد آلوده شده ، يافت مي شود . اين ناهمگوني معرف ميزان بالاي تكثير ويروس و ميزان بالاي خطاهاي ترانس كريپتاز معكوس است . بيشترين تنوع در بين ويروس هاي جدا شده ، در ناحيه ژن env ديده مي شود كه پروتيين هاي پوشش ويروس را رمزدهي مي كند . SU ، فرآورده ژنenv (gp120) ، حاوي قسمت هاي مسول اتصال ويروس به مولكول CD4 ، وگيرنده هايي است كه گرايش ويروس به لنفوسيت ها و ماكروفاژها را تعيين مي كند ، و شاخص هاي آنتي ژني عمده اي را كه بر عليه آنها ، آنتي بادي خنثي كننده توليد مي شود ، دارا مي باشد . گليكو پروتيين HIV داراي 5 ناحيه متغير (V) مي باشد كه در بين ويروس هاي جداسازي شده مختلف ، متنوع هستند . ناحيه V3 در خنثي سازي ويروس اهميت دارد . TM(gp41) ، فرآورده ژني env ، حاوي يك ناحيه خلال غشايي است كه گليكوپروتيين را به پوشش ويروس متصل مي كند ، و داراي يك ادغام كننده مي باشد كه نفوذ ويروس به داخل سلول هاي هدف را تسهيل م كند . وجود تنوع در پوشش HIV ، تلاش براي توليد يك واكسن مؤثر در برابر ايدز را با مشكل روبرو ساخته است . لنتي ويروس ها ، ويروس هايي كاملا اگزوژن (برون زاد ) هستند . بر خلاف رتروويروس هاي ترانس فرم كننده ، ژنوم لنتي ويروس ها ، هيچ گونه ژن سلولي را در بر ندارند . انسان با ورود ويروس از منابع خارجي به بدن، آلوده مي شود .
لنتي ويروس ها از تعداد زيادي از گونه ها ، جداسازي شده اند ، و 26 گونه متفاوت را در ميمون هاي انسان نماي آفريقا شامل مي شوند . دو ترتيب مجزا از عامل بيماري ايدز در انسان وجود دارد : HIV-1 و HIV-2 . اين دو تيپ ويروس را بر اساس ساختمان ژنوم و ارتباطات تكاملي با ساير لنتي ويروس هاي پريمات ها مي توان از هم افتراق داد . واگرايي توالي ژنوم بين HIV-1 و HIV-2 بيش از 50 در صد است .
بر اساس توالي ژن env، HIV-1 از سه گروه ويروسي متفاوت (M ، N وO ) تشكيل يافته است . گروه اصلي (M) حداقل 10 زير تيپ را شامل مي شود (A-J) . شكل هاي نو تركيب ويروس نيز در گردش خون افراد ساكن در نواحي مختلف جغرافيايي يافت شده اند . به طور مشابه 5 زير تيپ از HIV-2 (A تا E) شناسايي شده است . در هر زير تيپ تنوع زيادي وجود دارد . اين زير تيپ هاي ژنتيكي به نظر نمي رسد كه با گروه هاي سروتيپي خنثي سازي منطبق باشند و در حال حاضر شواهدي در تأييد تفاوت هاي بيولوژيك يا پاتوژنز بين زيرتيپ وجود ندارد .
لنتي ويروس هاي متعددي از گونه هاي مختلف ميمون هاي انسان نما ، جداسازي شده اند . لنتي ويروس هاي پريمات ها به 6 رده عمده تكاملي تقسيم مي شوند . SIV جدا شده از sooty mangabey( يك نوع ميمون در غرب آفريقا ) و HIV-2 ، به قدر كافي شباهت دارند كه بتوان آنها را به عنوان انواع يك ويروس به شمار آورد . ويروس هاي جدا شده از شمپانزه بيشتر به HIV-1 شباهت دارند . SIV هاي جدا شده از ميمون هاي سبز آفريقايي ، ميمون هاي sykes و mandrill ( شاه بابون ) ، و كولوبوس گروه هاي متمايزي را تشكيل مي دهند .
ساختمان ژنوم هاي لنتي ويروس هاي پريمات ها ( انسان و ميمون ) بسيار شبيه است . يك تفاوت اين است كه HIV-1 و ويروس شمپانزه ، ژن vpu را حمل مي كنند ، در حالي كه HIV-2 و SIV ها داراي ژن vpx هستند . ساير SIV هاي جدا شده فاقد هر دو ژن vpu و vpx هستند . توالي ژن هاي gag و pol به شدت حفظ شده است . بين ژن هاي گليكوپروتئين پوشش ويروس ، تنوع قابل توجهي وجود دارد ، توالي قسمت پروتئيني خلال غشايي ، بيشتر از توالي هاي مربوط به گليكوپروتئين خارجي ( جزء پروتئيني كه بر سطح خارجي ذره ويروسي وجود دارد )، حفظ شده است .
به نظر مي رسد ويروس هاي SIV در ميزبان هاي اصلي خود ( ميمون سبز آفريقايي ، شمپانزه sooty mangabey ) بيماريزا نيستند ، مشخص شده است كه اين گونه ها در محيط زندگي طبيعي خود ، به اين ويروس ها آلوده نمي شوند در مقابل ، ميمون هاي رزوس به طورمعمول ، در طبيعت در آسيا آلوده نمي شوند و نسبت به ايجاد ايدز ميموني ، در اثر انواع مختلف SIV حساس هستند . ويروسي كه اولين بار از ميمون هاي رزوس اسير شده ، جداسازي گرديد (SIVmac ) ، سويه HIV-2 / sooty mangabey بود .