پپتیدهای ضدمیکروبی ارگانیسم های چند سلولی
به طور کلی، ارگانیسم های چند سلولی در هماهنگی با میکروب ها زندگی می کنند. قرنیه ی چشم یک حیوان تقریبا” همیشه فاقد علایم عفونت است. حشره بدون لنفوسیت و پادتن رشد و نمو می کند. دانه ی گیاه به خوبی از بین میکروب های خاک جوانه می زند. چه طور این اتفاق می افتد؟ گیاهان و جانوران هر دو پپتیدهای ضدمیکروبی موثر و متنوعی دارند، که برای دفع انواع میکروب ها، از جمله باکتری ها، قارچ ها، ویروس ها و تک سلولی ها از آن ها استفاده می کنند. این پپتیدها چه نوع مولکول هایی هستند؟ چگونه جانوران برای دفاع از خود آن ها را به کار می گیرند؟ با توجه به این که نیاز به آنتی بیوتیک های جدید هر روزه بیش تر می شود، آیا می توانیم براساس طرحی که این مولکول ها ارائه می دهند، داروهای ضد عفونی طراحی کنیم؟
پپتیدهای ضد میکروبی سلاح های قدیمی (تکاملی) هستند. پراکنش گسترده ی آن ها در سرتاسر دنیای جانوران و حشرات نشان می دهد که پپتیدهای ضد میکروبی نقش حیاتی در تکامل موفقیت آمیز ارگانیسم های پیچیده ی چندسلولی دارند. علی رغم ، پپتیدهای ضد میکروبی هنوز هم سلاح های دفاعی موثری اند، و این باور عمومی را باطل می کنند که باکتری ها، قارچ ها و ویروس ها می توانند به هر ماده ی قابل تصوری مقاوم شوند. پپتیدهای ضدمیکروبی « پاشنه ی آشیل میکروب» را که خوب شناخته نشده هدف می گیرند، یعنی بخش اصلی طرح غشای سلولی میکروب که انواع میکروب ها را از جانوران و گیاهان چند سلولی متمایز می کند. شناخت حاصل از تحقیق گسترده، موجب تلاش تجاری بسیاری برای ابداع درمان های ضدعفونی جدید شده است.
تنوع پپتیدها
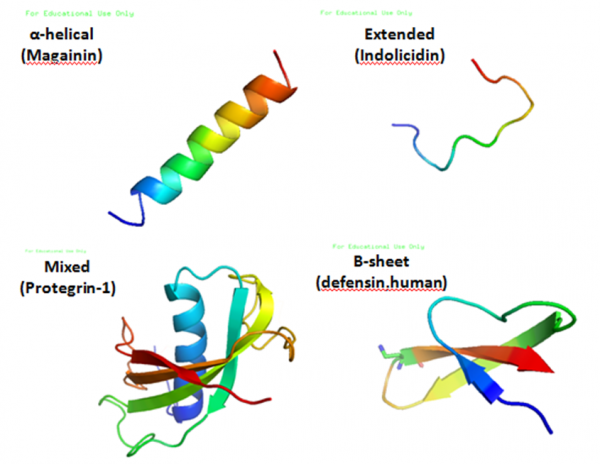
تنوع پپتیدهای ضدمیکروبی که کشف شده اند، آن قدر زیاد است که دسته بندی آن ها دشوار است؛ مگر دسته بندی کلی بر اساس ساختار فرعی آن ها. قائده ی ساختاری اصلی که زیربنای همه ی رده هاست، قابلیت مولکول در انتخاب ترکیبی است که از نظر مکانی خوشه های آمینواسیدهای هیدورفوبیک و کاتیونی در بخش های مجزایی از مولکول قرارمیگیرند(«آمفی پاتیک» ). پپتیدهای خطی، مانند سکروپینِ کرم ابریشم و ماگانینِ قورباغه ی چنگکیِ آفریقایی، این نظم را فقط زمانی اختیار می کنند که وارد غشا می شوند، و پس از آن ساختار ثانویه ی آلفا-هلیکال آمفی پاتیک را می پذیرند. این طرح در گونه های قورباغه از جنس رانا، با افزایش یک حلقه ی متشکل از پیوند دی سولفید به انتهایِ کربوکسی، ارتقا می یابد. پپتیدهایی مانند باکتنسین و دیفنسین صفحه ی بتاشیت غیرموازی نسبتا” سفتی هستند که پیوندهای دی سولفید مثل چارچوبی آن را محصور کرده است و در اطراف آن قطعات کاتیونی و هیدورفوبیایی قرار گرفته اند. یک خانواده ی بزرگ از پپتیدهای خطی که مشخصه ی آن غلبه ی یک یا دو آمینو اسید است (مانند ایندولیسیدینِ غنی از تریپتوفان در نوتروفیل گاو و PR39 غنی از پرولین-آرژینین در نوتروفیل خوک)، زنجیره های جانبی هیدورفوبیک و هیدورفیلیک را در اطراف داربست ممتد پپتید در محوطه ی غشا تفکیک می کند
در پی کشف انتشار گسترده ی پپتید ضدمیکروبی در طی20 سال گذشته، شناخت هایی نسبت به سیستم های دفاعی ذاتی حاصل شد که به ارگانیسم های چند سلولی، از جمله انسان ها امکان می دهد که با میکروب ها در سازگاری زندگی کنند. تصور این که اغلب جانورانی که اکنون زنده اند، از جمله حشرات و موجوداتی چون اختاپوس، و ستاره دریایی تا حد زیادی برای دفاع در برابر میکروب ها به پپتیدهای ضد میکروبی وابسته اند و این کار را بدون کمک لنفوسیت ها ، تیموس یا پادتن ها، بسیار خوب و موثر انجام می دهند (مخصوصا” پس از مطالعه ی متون قدیمی ایمنی شناسی) دشوار است. اگر این تنوع بر اساس مشاهدات کنونی ما همچنان بیش تر شود، ممکن است به خوبی متوجه شویم که هر گونه، مجموعه پپتیدهای ضدمیکروبی منحصر به فرد و مخصوص به خودی دارد که برای دفاع از ارگانیسم در برابر میکروارگانیسم هایی تنظیم شده اند که احتمالا” با آن مواجه می شود. مولکول هایی که به تازگی توصیف شده اند، طرح های مولکولی را برای ایجاد درمان های جدید الهام می کنند و با کشفیات بیشتر، درمان های جدیدتری ابداع می شود، زیرا این مولکول ها بر اساس راه کارهای ضدمیکروبی کار می کنند که طی چندین هزاره ثابت و موثر بوده است. تحقیقات در آزمایشگاه و در کلینیک تایید می کند که احتمال پیدایش مقاومت در برابر پپتیدهای ضدمیکروبی نسبت به آن چه در مورد آنتی بیوتیک های متداول مشاهده شده، کم تر است که انگیزه ی ایجاد پپتیدهای ضدمیکروبیِ طبیعی و آزمایشگاهی، را در عوامل مفید درمانی ایجاد می کند.